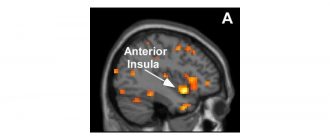
Eine neue Entdeckung darüber, wie der Körper rote Blutkörperchen produziert, könnte zu einer verbesserten Behandlung von Anämie führen.
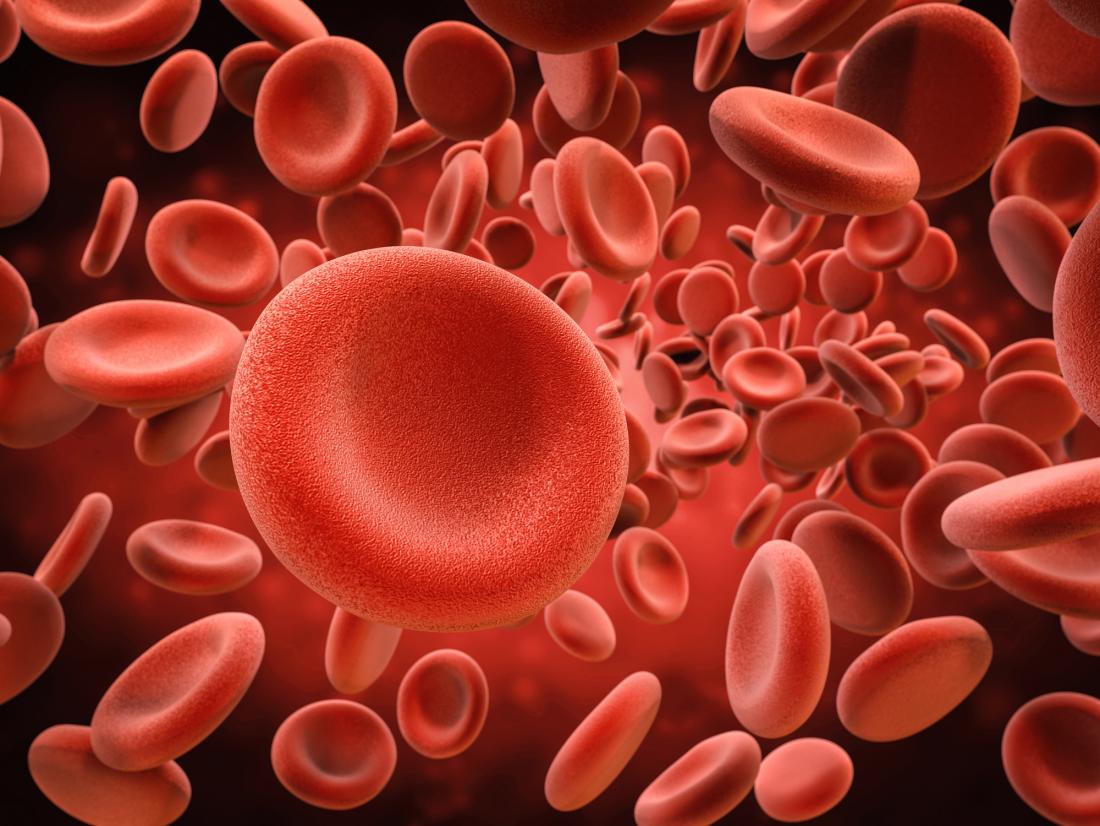
Forscher an der medizinischen Fakultät der Universität von Virginia in Charlottesville machten die Entdeckung, während sie untersuchten, warum der Körper nicht genug rote Blutkörperchen in Eisen-eingeschränkten Anämien machen kann.
Sie berichten von ihren Befunden, die die Rolle des Hormons Erythropoietin (EPO) bei der Produktion roter Blutkörperchen betreffen.
Anämie ist eine Blutkrankheit, bei der entweder der Körper nicht genügend rote Blutkörperchen hat, um Sauerstoff zu den Geweben zu transportieren, oder die roten Blutkörperchen fehlerhaft sind und ihre Aufgabe nicht richtig erfüllen können. Dies kann zu Schwäche, Müdigkeit, Konzentrationsschwäche und anderen Symptomen führen.
Weltweit ist Anämie ein großes Gesundheitsproblem, von dem mehr als 1,6 Milliarden Menschen betroffen sind.
In den Vereinigten Staaten ist Anämie ein "wachsendes Problem". Die Prävalenz hat sich im Zeitraum 2003-2004 bis 2011-2012 von 4 Prozent auf 7 Prozent nahezu verdoppelt.
Eisen, rote Blutkörperchen und EPO
Es gibt viele Arten und Ursachen von Anämie. Am häufigsten sind Eisenmangel, den der Körper benötigt, um Hämoglobin, das Protein in roten Blutkörperchen, zu bilden, das ihnen hilft, Sauerstoff zu transportieren.
Eisen ist auch für andere biologische Funktionen wichtig, und der Körper hat mehrere Wege entwickelt, um das Element zu erhalten, einschließlich des Recyclings aus zerlegten roten Blutkörperchen.
Zu viel Eisen kann giftig sein, und der Körper verfügt über Mechanismen, die dafür sorgen, dass es in einem sicheren Bereich bleibt. Zum Beispiel begrenzt es Absorption und erfüllt den größten Teil seines täglichen Bedarfs durch Recycling.
Rote Blutkörperchen werden im Knochenmark in einem komplizierten Prozess hergestellt, der vom Hormon EPO kontrolliert wird.
EPO sendet Anweisungen an Knochenmarksstammzellen, die sie über EPO-Rezeptoren auf ihren Außenflächen erhalten.
EPO-Rezeptoren müssen außerhalb von Zellen sein
Der Hauptautor Shadi Khalil, ein Doktorand in der Arbeitsgruppe von Prof. Goldfarb, bemerkte jedoch etwas Überraschendes bei der Untersuchung von Knochenmarkszellen im Labor: Er bemerkte, dass sie viel EPO-Rezeptor in sich, aber nicht auf ihrer Außenfläche enthielten.
Dies veranlasste ihn zu der Frage, ob der Grund dafür, dass EPO-Hormonanweisungen bei einigen Menschen fehlschlagen, darin liegt, dass ihre Knochenmarkzellen nicht genug EPO-Rezeptoren auf ihren Oberflächen haben.
Nach einigen Tests an Mäusen fanden die Forscher die Antwort auf die Frage – zumindest teilweise. Sie fanden heraus, dass "Mäuse mit erzwungener Oberflächenretention des Rezeptors keine Anämie mit Eisenmangel entwickeln".
Es gab jedoch noch ein anderes Teil des Puzzles zu finden.
Erkenntnisse können zu neuen Behandlungen führen
Es stellte sich heraus, dass ein anderes Mitglied des Teams bereits an dem fehlenden Teil arbeitete. Diese Arbeit zeigte, dass, wenn die Eisenspiegel zu niedrig fallen, ein bestimmtes Protein, das den EPO-Rezeptor reguliert, verschwindet. Das Protein, das vom SCRIB-Gen kodiert wird, heißt Scribble.
"Scribble-Defizienz reduziert die Oberflächenexpression des Epo-Rezeptors, behält aber selektiv die Überlebenssignalisierung bei", bemerken die Autoren.
Mit anderen Worten, sie entdeckten, dass Eisenspiegel im Blut das Niveau von Scribble beeinflussen, was wiederum entscheidet, ob sich EPO-Rezeptoren innerhalb oder außerhalb der Knochenmarkzellen ansammeln.
"Wir haben realisiert", erklärt Khalil, "dass dies eine Art komplizierte Symphonie war, die mit Eisen anfängt und letztlich kontrolliert, wie viel und welche Art von Botschaften die Zellen bekommen."
Die Forscher hoffen, dass ihre Entdeckungen zur "Fixierung der EPO-Resistenz" zu neuen Behandlungsmethoden für Anämie führen werden.
"Wir haben die Schlüsselkomponenten", resümiert Prof. Goldfarb die Ergebnisse und zeigt auf den nächsten Schritt, "und wir wollen die Hierarchie auf das regulatorische Masterelement aufsetzen, das dies steuert."
"Wenn wir das tun, wird uns das den alternativen Behandlungsmethoden für Anämie viel näher bringen."
Prof. Adam N. Goldfarb