In einer Sicherheitsankündigung hat die amerikanische Gesundheitsbehörde FDA (Food and Drug Administration) das Etikett für das verschreibungspflichtige Medikament Chantix aktualisiert und davor gewarnt, dass es die Reaktion des Körpers auf Alkohol verändern und in seltenen Fällen zu Krampfanfällen führen könnte.
Pfizer, der Hersteller von Chantix (Vareniclin), reichte eine Fallserie bei der Food and Drug Administration (FDA) ein, die zusammen mit gemeldeten Fällen von Patienten, die unerwünschte Reaktionen auf das Medikament hatten, von der FAERS-Datenbank (FDA Adverse Event Reporting System) überprüft wurde.
Chantix ist ein weit verbreitetes Medikament zur Raucherentwöhnung, das 2006 von der FDA zugelassen wurde. Die FDA gibt an, dass im Jahr 2013 schätzungsweise 1,2 Millionen Patienten ein Rezept für Chantix von ambulanten Apotheken in den USA erhalten haben.
"In klinischen Studien hat Chantix die Wahrscheinlichkeit, mit dem Rauchen aufzuhören, um 1 Jahr im Vergleich zur Behandlung mit einem Placebo, einer inaktiven Behandlung, zu verlängern", schreiben die FDA.
Das National Cancer Institute (NCI) berichtet, dass Tabakkonsum die häufigste Ursache für vermeidbare Krankheit und Tod in den USA ist. Zigarettenrauchen allein verursacht ungefähr 443.000 Todesfälle pro Jahr, einschließlich geschätzter 49.000 Todesfälle, die auf Passivrauchen zurückzuführen sind.
Aufgrund der ernsten Gesundheitsprobleme, die durch Rauchen verursacht werden können, wie Krebs und Herz-Kreislauf-Erkrankungen, könnte Chantix ein wichtiges Medikament sein, das Tausende von Amerikanern vor chronischen Gesundheitsproblemen schützt. Die aktualisierte Kennzeichnung des Arzneimittels wird Patienten und Ärzte gleichermaßen dazu veranlassen, sich mit ein wenig mehr Vorsicht an sie zu wenden.
FDA gibt an, dass Anfälle von Patienten berichtet wurden, die mit Chantix behandelt wurden
In einem Rückblick auf die von Pfizer und der FAERS-Datenbank präsentierte Fallserie stellte die FDA fest, dass bei Patienten, die während der Behandlung mit Chantix Alkohol getrunken haben, eine Reihe von Nebenwirkungen aufgetreten sind.
Diese Nebenwirkungen standen im Zusammenhang mit einer verminderten Toleranz für Alkohol und beinhalteten eine erhöhte Intoxikation, Gedächtnisverlust und aggressives oder uncharakteristisches Verhalten.
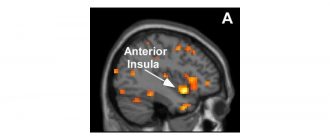
Darüber hinaus identifizierte die FDA in ihrer Überprüfung der FAERS-Datenbank Fälle von Patienten, die von Chantix mit Krampfanfällen behandelt wurden, die entweder keine Anfälle in der Anamnese oder eine gut kontrollierte Anfallsstörung hatten. Die FDA stellte fest, dass die Mehrzahl dieser Fälle innerhalb des ersten Behandlungsmonats auftraten.
Der Abschnitt "Warnhinweise und Vorsichtsmaßnahmen" auf dem Etikett des Arzneimittels wird nun aktualisiert, um Informationen über diese Risiken sowie zusätzliche Informationen aus Beobachtungsstudien, die das Risiko von Chantix auf die Stimmung und das Verhalten der Patienten beeinflussen, zu erhalten.
Obwohl die von Pfizer durchgeführten Beobachtungsstudien und randomisierten kontrollierten klinischen Studien kein erhöhtes Risiko für neuropsychiatrische Nebenwirkungen aufwiesen, wiesen sie jeweils Einschränkungen auf, die die FDA daran hinderten, zu verlässlichen Schlussfolgerungen zu kommen.
Als Reaktion auf diese neu gefundenen Risiken empfiehlt die FDA, dass Patienten, die mit Chantix behandelt werden, die Menge an Alkohol reduzieren sollten, die sie konsumieren, bis sie wissen, in welchem Ausmaß das Medikament ihre Fähigkeit, Alkohol zu tolerieren, beeinflusst.
Vor der Einnahme von Chantix wird den Patienten empfohlen, ihren Arzt darüber zu informieren, wenn sie in der Vergangenheit Krampfanfälle hatten, Alkohol getrunken haben oder in der Vergangenheit psychische Probleme hatten.
Patienten sollten nach Verhaltensänderungen oder Denkweisen Ausschau halten, die für sie untypisch sind, da diese möglicherweise Nebenwirkungen der Medikamente sein können. "Wir fordern Ärzte und Patienten auf, Nebenwirkungen von Chantix beim FDA MedWatch-Programm zu melden", schließt die FDA.
Letzten Monat wurde über eine Studie berichtet, die darauf hindeutet, dass mehrere Bedenken bezüglich betrügerischer klinischer Studien, die der FDA bekannt sind, nicht für Zeitschriften oder Patienten veröffentlicht wurden.