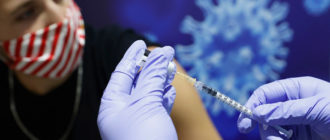
Tamiflu und Relenza sind Medikamente, die häufig zur Vorbeugung und Behandlung von Influenza bei Erwachsenen und Kindern eingesetzt werden. Frühere Forschung hat die Medikamente für die Verringerung der Krankenhausaufnahmen und Komplikationen als Folge des Virus gefeiert. Aber in der letzten Cochrane Review, die kürzlich in der Zeitschrift "Cochrane Review" veröffentlicht wurde, sagen die Forscher, dass es keine stichhaltigen Beweise für solche Behauptungen gibt.
Tamiflu (Oseltamivir) und Relenza (Zanamivir) sind Arzneimittelklassen, die als Neuraminidasehemmer bekannt sind. Beide Medikamente sollen die Grippesymptome verhindern und reduzieren, indem sie das Influenzavirus daran hindern, sich im Körper zu verbreiten.
Gegenwärtig wird Tamiflu zur Behandlung der Grippe bei Patienten im Alter von 2 Wochen und älter angewendet, deren Symptome nicht länger als 2 Tage anhielten. Es kann verwendet werden, um Grippe bei Patienten ab 1 Jahr zu verhindern. Relenza wird zur Behandlung von Grippe bei Patienten ab 7 Jahren eingesetzt und kann zur Grippeprävention bei Personen ab 5 Jahren angewendet werden.
Laut den Forschern, die an diesem letzten Bericht beteiligt waren, darunter Dr. Carl Heneghan von der Universität Oxford in Großbritannien und Dr. Peter Doshi von der University of Maryland Pharmazie in den USA, werden beide Medikamente gegen saisonale und pandemische Krankheiten gelagert Grippe. Zum Beispiel haben die USA mehr als 1,3 Milliarden US-Dollar für Reserven an antiviraler Influenza ausgegeben.
Diese Lagerhaltung basierte auf internationalen und nationalen Empfehlungen von Einrichtungen wie der Weltgesundheitsorganisation (WHO) und den Zentren für Krankheitskontrolle und -prävention (CDC). Aber worauf basieren ihre Empfehlungen?
Das Team sagt, dass die Empfehlungen des Neuraminidasehemmers für die Europäische CDC auf einer Zusammenfassung der Vorteile und Schädigungen der Europäischen Arzneimittelagentur (EMA) beruhten, während andere Empfehlungen auf den Ergebnissen von Studien von Arzneimittelherstellern wie GlaxoSmithKline basierten ( GSK).
Im Jahr 2009 versuchten Cochrane-Forscher, die Sicherheit und Wirksamkeit von Neuraminidasehemmern zu überprüfen. Die Arzneimittelhersteller verweigerten jedoch den vollständigen Zugang zu den Daten der klinischen Studien über die Arzneimittel, was ihre Bemühungen behinderten.
Dies wirft die Frage auf, ob die Risiken und Vorteile von antiviralen Influenza-Impfstoffen genau berichtet wurden und ob sie für die Behandlung der saisonalen und pandemischen Grippe bei Kindern und Erwachsenen gelagert werden sollten.
Im Jahr 2012 berichtete eine Geschichte, wie Roche – die Hersteller von Tamiflu – unter Druck gesetzt wurden, Probendaten für das Medikament zu veröffentlichen.
Nachdem die Forscher nun Zugang zu den Daten der ursprünglichen klinischen Studie hatten, konnten sie 20 vollständige interne Berichte über die Auswirkungen von Tamiflu und 26 Berichte über die Auswirkungen von Relenza analysieren. Insgesamt umfassten die Berichte mehr als 24.000 Menschen.
Befunde stellen Nutzen und Risiken von Influenza-Virostatika in Frage
Bei der Überprüfung der Vorteile von Tamiflu fanden die Forscher heraus, dass das Medikament zu einer schnelleren Linderung der Grippesymptome um nur einen halben Tag (von 7 Tagen auf 6,3 Tage) führte, verglichen mit einem Placebo-Medikament.
Tamiflu hat bei Erwachsenen oder Kindern keine Krankenhausaufenthalte oder Komplikationen durch schwere Grippe – wie Lungenentzündung, Bronchitis, Sinusitis oder Ohrenentzündung – reduziert.
Die Forscher fanden heraus, dass das Medikament Übelkeit und Erbrechen bei Erwachsenen und Kindern um 4% bzw. 5% erhöht. Als Tamiflu zur Vorbeugung der Influenza eingesetzt wurde, stieg das Risiko psychiatrischer Ereignisse um 1%. Diese Effekte wurden in den ersten klinischen Studien nicht berichtet.
Außerdem stellte das Team fest, dass Tamiflu einige Menschen daran hinderte, genug eigene Antikörper gegen die Grippeinfektion zu produzieren.
Dr. David Tovey, Chefredakteur bei Cochrane, kommentiert diese Erkenntnisse wie folgt:
"Ursprünglich wurde erwogen, Hospitalisierungen und ernsthafte Komplikationen durch Influenza zu reduzieren, die Überprüfung zeigt jedoch, dass Tamiflu nicht nachweislich dazu in der Lage ist, und es scheint auch zu schädlichen Auswirkungen zu führen, die in den ursprünglichen Veröffentlichungen nicht vollständig beschrieben wurden Studiendaten sind transparent und zugänglich. "
Die Ergebnisse waren für Relenza ähnlich. Es wurde festgestellt, dass das Medikament die Dauer der Grippesymptome bei Erwachsenen von 6,6 auf 6 Tage reduzierte – das entspricht 14,4 Stunden – im Vergleich zu einem Placebo-Medikament. Keine signifikante Wirkung wurde bei Kindern gefunden.
Das Team fand keine Beweise, dass Relenza das Risiko von Grippekomplikationen oder das Risiko eines Krankenhausaufenthaltes reduziert.
"Empfehlungen für Tamiflu und Relenza sollten überarbeitet werden"
Basierend auf ihren Ergebnissen, sagen die Forscher, dass Empfehlungen zur Verwendung von Tamiflu und Relenza zur Vorbeugung oder Behandlung von Influenza überarbeitet werden sollten.
"Die Zulassung und Verwendung von Medikamenten kann nicht länger auf voreingenommenen oder fehlenden Informationen basieren. Wir riskieren zu viel in der Gesundheit und Wirtschaft unserer Bevölkerung", so die Autoren.
Sie weisen darauf hin, dass dieser aktualisierte Cochrane Review der erste ist, der nur auf klinischen Studien und Kommentaren der Regulierungsbehörden basiert, was bedeutet, dass die Ergebnisse "viel reicher" sind.
"Wir fordern die Menschen auf, nicht auf veröffentlichte Studien allein oder auf Kommentare von konfliktbehafteten Entscheidungsträgern im Gesundheitswesen zu vertrauen, sondern die Informationen für sich selbst zu sehen", fügen sie hinzu.
Dr. Tovey, Chefredakteurin Fiona Godlee und die klinische Redakteurin Elizabeth Loder, weisen in einem mit den Übersichtsartikeln verknüpften Leitartikel darauf hin, dass die Ergebnisse dieser Übersicht die Notwendigkeit unterstreichen, alle Daten aus klinischen Studien für derzeit in Deutschland verfügbare Arzneimittel zur Verfügung zu stellen verwenden, damit alle Informationen genau bewertet werden können.
"Die außergewöhnlichen Bemühungen der Cochrane-Reviewer haben erreicht, was Routine sein sollte – die unabhängige Prüfung von Daten aus klinischen Studien", fügen sie hinzu.
"Sie haben deutlicher denn je gezeigt, dass das derzeitige System gebrochen ist.Es gibt noch erhebliche Kämpfe, die es zu bekämpfen gilt, bevor wir ein System der Drogenbewertung und -emulation haben, das den Patienten und dem öffentlichen Interesse wirklich dient. "