Klinische Studien sind Forschungsstudien, die darauf abzielen, festzustellen, ob eine medizinische Strategie, Behandlung oder ein Gerät für die Verwendung oder den Verzehr durch den Menschen sicher ist.
Diese Studien können auch bewerten, wie effektiv ein medizinischer Ansatz für bestimmte Bedingungen oder Gruppen von Menschen ist.
Insgesamt tragen sie zu medizinischem Wissen bei und liefern verlässliche Daten zur Entscheidungsfindung und Richtlinien für die Gesundheitsversorgung.
Um die Sicherheit der Teilnehmer zu gewährleisten, beginnen die Versuche mit kleinen Gruppen und untersuchen, ob eine neue Methode schädliche oder unbefriedigende Nebenwirkungen verursacht. Dies liegt daran, dass eine Technik, die in einem Labor oder bei Tieren erfolgreich ist, für den Menschen möglicherweise nicht sicher oder wirksam ist.
Schnelle Fakten zu klinischen Studien
- Klinische Studien zielen darauf ab herauszufinden, ob eine medizinische Strategie, Behandlung oder ein Gerät sicher und effektiv für den Menschen ist, zu verwenden oder zu konsumieren.
- Trials bestehen aus vier Phasen und können sich auf Folgendes konzentrieren: Behandlung, Prävention, Diagnose, Screening, unterstützende Versorgung, Forschung im Gesundheitswesen und Grundlagenforschung.
- Ein Forschungsteam wird wahrscheinlich Ärzte, Krankenschwestern, Sozialarbeiter, Angehörige der Gesundheitsberufe, Wissenschaftler, Datenmanager und Koordinatoren für klinische Studien umfassen.
- Partizipation kann sowohl Risiken als auch Vorteile mit sich bringen. Die Teilnehmer müssen das "informed consent" -Dokument lesen und unterzeichnen, bevor sie einer Testversion beitreten.
- Risiken werden kontrolliert und überwacht, aber die Art von medizinischen Forschungsstudien bedeutet, dass einige Risiken unvermeidlich sind.
Was sind klinische Studien?
Der Hauptzweck von klinischen Studien ist Forschung. Studien sollen das medizinische Wissen in Bezug auf die Behandlung, Diagnose und Prävention von Krankheiten oder Zuständen erweitern.

Studien folgen strengen wissenschaftlichen Standards und Richtlinien, die darauf abzielen:
- Teilnehmer schützen
- liefern zuverlässige und genaue Ergebnisse
Klinische Studien am Menschen finden in den letzten Phasen eines langen, systematischen und gründlichen Forschungsprozesses statt.
Der Prozess beginnt oft in einem Labor, wo neue Konzepte entwickelt und getestet werden.
Durch Tierversuche können Wissenschaftler sehen, wie sich der Ansatz auf einen lebenden Körper auswirkt.
Schließlich werden menschliche Tests in kleinen und dann in größeren Gruppen durchgeführt.
Versuche können durchgeführt werden:
- Bewerten Sie eine oder mehrere Behandlungsmaßnahmen für eine Krankheit, ein Syndrom oder einen Zustand, z. B. Medikamente, medizinische Geräte oder Ansätze für Operationen oder Therapien
- Bewerten Sie Wege, um eine Krankheit oder einen Zustand zu verhindern, zum Beispiel durch Medikamente, Impfstoffe und Lebensstiländerungen
- Bewerten Sie einen oder mehrere Diagnose-Interventionen, die eine bestimmte Krankheit oder einen bestimmten Zustand identifizieren oder diagnostizieren könnten
- Untersuchen Sie Identifizierungsmethoden, um eine Bedingung oder Risikofaktoren für diese Bedingung zu erkennen
- Erkunden Sie unterstützende Pflegeverfahren, um den Komfort und die Lebensqualität von Menschen mit einer chronischen Krankheit zu verbessern
Das Ergebnis einer klinischen Studie kann identifizieren, ob eine neue medizinische Strategie, Behandlung oder ein neues Gerät:
- wirkt sich positiv auf die Prognose des Patienten aus
- verursacht unvorhergesehenen Schaden
- hat keinen positiven Nutzen oder hat negative Auswirkungen
Klinische Studien können wertvolle Informationen über die Kosteneffektivität einer Behandlung, den klinischen Wert eines diagnostischen Tests und darüber, wie eine Behandlung die Lebensqualität verbessert, liefern.
Arten der klinischen Prüfung
Alle klinischen Studien haben einen Hauptzweck. Diese können in folgende Kategorien unterteilt werden:
- Behandlung: Testen neuer Behandlungen, neuer Medikamentenkombinationen oder neuer Ansätze in der Chirurgie oder Therapie
- Prävention: Untersuchung von Möglichkeiten zur Verbesserung der Vorbeugung oder Wiederholung von Krankheiten, beispielsweise durch Medikamente, Vitamine, Impfstoffe, Mineralstoffe und Veränderungen des Lebensstils
- Diagnose: Suche nach verbesserten Testtechniken und -verfahren zur Diagnose von Krankheiten und Zuständen
- Screening: Testen der besten Methode zur Identifizierung bestimmter Krankheiten oder Gesundheitszustände
- Unterstützende Versorgung: Untersuchung von Verfahren zur Verbesserung des Komforts und der Lebensqualität von Patienten mit chronischen Erkrankungen
- Versorgungsforschung: Bewertung der Lieferung, des Prozesses, des Managements, der Organisation oder der Finanzierung des Gesundheitswesens
- Grundlagenforschung: Untersuchen, wie eine Intervention funktioniert
Warum sind klinische Studien wichtig?
Klinische Studien helfen, die medizinische Versorgung zu verbessern und voranzutreiben. Die Studien liefern Fakten, die zur Verbesserung der Patientenversorgung genutzt werden können.
Klinische Forschung wird nur durchgeführt, wenn Ärzten Elemente wie:
- ob ein neuer Ansatz effektiv bei Menschen funktioniert und sicher ist
- Welche Behandlungen oder Strategien arbeiten am erfolgreichsten für bestimmte Krankheiten und Gruppen von Individuen?
Wie funktionieren klinische Studien?
An der Einrichtung, Durchführung und Weiterverfolgung einer klinischen Studie sind verschiedene Elemente beteiligt.
Protokoll für klinische Studien

Eine Studie folgt einem umfassenden Plan oder Protokoll. Ein Protokoll ist die schriftliche Beschreibung einer klinischen Studie.
Es beinhaltet Ziele, Design und Methoden der Studie, relevanten wissenschaftlichen Hintergrund und statistische Informationen.
Zu den wichtigsten Informationen gehören:
- die Anzahl der Teilnehmer
- wer kann teilnehmen?
- Welche Tests werden gegeben und wie oft?
- Arten von Daten gesammelt werden
- die Länge der Studie
- detaillierte Informationen zum Behandlungsplan
Verzerrungen vermeiden
Die Forscher müssen Maßnahmen ergreifen, um Verzerrungen zu vermeiden.
Bias bezieht sich auf menschliche Entscheidungen oder andere Faktoren, die nicht mit dem Protokoll zusammenhängen, aber die Ergebnisse der Studie beeinflussen können.
Schritte zur Vermeidung von Verzerrungen sind Vergleichsgruppen, Randomisierung und Maskierung.
Vergleichsgruppen
Die meisten klinischen Studien verwenden Vergleichsgruppen, um medizinische Strategien und Behandlungen zu vergleichen. Die Ergebnisse zeigen, ob eine Gruppe ein besseres Ergebnis hat als die andere.
Dies wird normalerweise auf zwei Arten durchgeführt:
- Eine Gruppe erhält eine bestehende Behandlung für eine Erkrankung und die zweite Gruppe erhält eine neue Behandlung. Die Forscher vergleichen dann, welche Gruppe bessere Ergebnisse erzielt.
- Eine Gruppe erhält eine neue Behandlung, und die zweite Gruppe erhält ein Placebo, ein inaktives Produkt, das wie das Testprodukt aussieht.
Randomisierung
Klinische Studien mit Vergleichsgruppen verwenden häufig Randomisierung. Die Teilnehmer werden zufällig und nicht nach Wahl den Vergleichsgruppen zugeteilt. Dies bedeutet, dass jegliche Unterschiede, die während einer Testphase auftreten, auf die verwendete Strategie zurückzuführen sind und nicht auf vorher bestehende Unterschiede zwischen den Teilnehmern.
Maskierung oder Verblindung
Maskierung oder Verblindung hilft, Verzerrungen zu vermeiden, indem weder die Teilnehmer noch die Forscher darüber informiert werden, welche Behandlung die Teilnehmer erhalten werden.
Single Blind: Dies ist, wenn entweder die Teilnehmer oder Forscher nicht wissen, welche Gruppe welche ist.
Doppelblind: Dies ist, wenn sowohl Teilnehmer als auch Forscher nichts wissen.
Störende Faktoren
Ein Confounder kann die wahre Beziehung zwischen zwei oder mehr Merkmalen verzerren.
Zum Beispiel könnte man folgern, dass Menschen, die einen Zigarettenanzünder tragen, eher Lungenkrebs entwickeln, weil das Tragen eines Feuerzeugs Lungenkrebs verursacht. Rauchen ist in diesem Beispiel ein Confounder.
Menschen, die einen Zigarettenanzünder tragen, sind eher Raucher, und Raucher entwickeln wahrscheinlicher Lungenkrebs, aber manche Menschen können ein Feuerzeug für andere Zwecke tragen.
Wird dies nicht berücksichtigt, kann dies zu falschen Schlussfolgerungen führen.
Wer ist im Forschungsteam?
Ein Hauptprüfer, normalerweise ein Arzt, wird jede klinische Studie leiten.
Das Forschungsteam kann umfassen:
- Ärzte
- Krankenschwestern
- Sozialarbeiter
- medizinische Fachkräfte
- Wissenschaftler
- Datenmanager
- Koordinatoren für klinische Studien
Wo werden klinische Studien durchgeführt?
Der Standort hängt von der Art des Studiums und von der Organisation ab.
Einige häufige Orte sind:
- Krankenhäuser
- Universitäten
- medizinische Zentren
- Arztpraxen
- Gemeinschaftskliniken
- Bundesfinanzierte und von der Industrie geförderte Forschungsstandorte
Wie lange dauern die Studien?
Dies hängt unter anderem davon ab, was untersucht wird. Einige Versuche letzten Tage, während andere für Jahre fortfahren.
Vor der Teilnahme an einer Studie wird den Teilnehmern mitgeteilt, wie lange sie voraussichtlich dauern wird.
Design und Organisation
Es gibt verschiedene Arten von Studien und verschiedene Arten, sie zu organisieren. Hier sind einige Studientypen.
Beobachtende Studien
Kohortenstudien und Fallkontrollstudien sind Beispiele für Beobachtungsstudien.
Kohortenstudie

Eine Kohortenstudie ist eine Beobachtungsstudie, in der die Studienpopulation oder Kohorte ausgewählt wird.
Es werden Informationen gesammelt, um festzustellen, welche Fächer entweder
- B. eine Blutgruppe, von der angenommen wird, dass sie mit der Entwicklung der betreffenden Krankheit in Zusammenhang steht
- Exposition gegenüber einem Faktor, der mit einer Krankheit in Verbindung gebracht werden kann, z. B. Zigarettenrauchen
Eine Person könnte gewählt werden, weil sie rauchen. Sie können dann rechtzeitig verfolgt werden, um zu sehen, wie wahrscheinlich es ist, eine Krankheit zu entwickeln, verglichen mit anderen Menschen.
Diese Art von Studie wird verwendet, um die Wirkung von vermuteten Risikofaktoren zu untersuchen, die experimentell nicht kontrolliert werden können, wie zum Beispiel die Auswirkungen des Rauchens auf Lungenkrebs.
Die Hauptvorteile von Kohortenstudien sind:
- Die Exposition wird vor dem Ausbruch der Krankheit gemessen und ist daher wahrscheinlich hinsichtlich der Krankheitsentwicklung unvoreingenommen.
- Seltene Expositionen können durch geeignete Auswahl von Studienkohorten untersucht werden.
- Mehrere Ergebnisse – oder Krankheiten – können für jede einzelne Exposition untersucht werden.
- Die Krankheitsinzidenz kann sowohl in der exponierten als auch in der unbelichteten Gruppe berechnet werden.
Die Hauptnachteile von Kohortenstudien sind:
- Sie sind in der Regel teuer und zeitaufwändig, insbesondere wenn sie prospektiv durchgeführt werden, was bedeutet, dass sie sich vorwärts bewegen.
- Änderungen des Expositionsstatus und der diagnostischen Kriterien im Laufe der Zeit können die Einstufung von Personen je nach Exposition und Krankheitsstatus beeinflussen.
- Es könnte zu Informationsverzerrungen im abgeschlossenen Ergebnis kommen, da der Expositionsstatus des Probanden bekannt ist.
- Zu erwartende Verluste können eine Selektionsverzerrung darstellen.
Fallkontrollstudien
Eine Fall-Kontroll-Studie kann Risikofaktoren für eine bestimmte Erkrankung unterscheiden.
Forscher vergleichen Menschen mit einer Krankheit und solche ohne sie. Indem sie rückwärts arbeiten, identifizieren sie, wie sich die beiden Gruppen unterscheiden.
Fall-Kontroll-Studien sind immer rückblickend – rückwärts schauend – weil sie mit dem Ergebnis beginnen und dann zurückverfolgen, um die Exposition zu untersuchen.
Die Hauptvorteile von Fall-Kontroll-Studien sind:
- Ergebnisse können schnell erhalten werden.
- Die Studie kann mit einem Minimum an Finanzierung oder Sponsoring stattfinden.
- Sie sind effizient für die Untersuchung seltener Krankheiten oder Krankheiten mit einer langen Induktionszeit.
- Ein breites Spektrum möglicher Risikofaktoren kann untersucht werden.
- Mehrfachbelichtungen können untersucht werden.
- Sie erfordern wenige Studienfächer.
Die Hauptnachteile von fallkontrollierten Studien sind:
- Inzidenzdaten können nicht generiert werden.
- Sie unterliegen einer Verzerrung.
- Es kann schwierig sein, genaue, unverzerrte Messungen früherer Expositionen zu erhalten, wenn die Aufzeichnungen unzureichend oder unzuverlässig sind. Dies wird Information Bias genannt.
- Die Auswahl von Steuerelementen kann problematisch sein. Dies kann zu einer Auswahlverzerrung führen.
- Die chronologische Abfolge zwischen Exposition und Krankheit kann schwer zu identifizieren sein.
- Sie sind nicht geeignet, seltene Expositionen zu untersuchen, es sei denn, die Exposition ist für einen Großteil der Fälle verantwortlich.
Verschachtelte Fall-Kontroll-Studie
In einer verschachtelten Fall-Kontroll-Studie stammen die Gruppen – Fälle und Kontrollen – aus derselben Studienpopulation oder -kohorte.
Wenn die Kohorte weiterverfolgt wird, werden die Fälle, die auftreten, die "Fälle" in der Fall-Kontroll-Studie. Die nicht betroffenen Teilnehmer der Kohorte werden zu den "Kontrollen".
Verschachtelte Fall-Kontroll-Studien sind im Vergleich zu einer Kohortenstudie weniger kostspielig und weniger zeitaufwendig.
Inzidenz- und Prävalenzraten der Krankheit können gelegentlich aus einer verschachtelten Fall-Kontroll-Kohortenstudie projiziert werden. Dies ist aus einer einfachen Fall-Kontroll-Studie nicht möglich, da die Gesamtzahl der exponierten Personen und die Nachbeobachtungszeiten normalerweise unbekannt sind.
Die Hauptvorteile verschachtelter Fall-Kontroll-Studien sind:
- Effizienz: Nicht alle Teilnehmer der Kohorte benötigen diagnostische Tests.
- Flexibilität: Sie ermöglichen das Testen von Hypothesen, die bei der Planung der Kohorte nicht erwartet wurden.
- Verringerung der Selektionsverzerrung: Fälle und Kontrollen werden aus derselben Population entnommen.
- Verringerung des Informationsbias: Die Exposition des Risikofaktors kann mit dem Blind-to-Case-Status des Prüfers bewertet werden.
Der Hauptnachteil besteht darin, dass die Ergebnisse aufgrund der geringen Stichprobengröße weniger Autorität haben.
Ökologische Studie
Eine ökologische Studie untersucht die Beziehung zwischen Exposition und Ergebnis der Bevölkerung oder Gemeinschaft.
Gemeinsame Kategorien der ökologischen Studie umfassen:
- geografische Vergleiche
- Zeit-Trend-Analyse
- Migrationsstudien
Die wesentlichen Vorteile ökologischer Studien sind:
- Sie sind kostengünstig, da routinemäßig erhobene Gesundheitsdaten genutzt werden können.
- Sie sind weniger zeitaufwendig als andere Studien.
- Sie sind unkompliziert und einfach zu verstehen.
- Die Auswirkungen von Expositionen, die über Gruppen oder Bereiche gemessen werden – wie Ernährung, Luftverschmutzung und Temperatur – können untersucht werden.
Die Hauptnachteile ökologischer Studien sind:
- Fehler der Ableitung, die als ökologischer Fehlschluss bekannt sind, können auftreten. Dies geschieht, wenn Forscher auf der Basis von Gruppendaten ausschließlich Rückschlüsse auf Individuen ziehen.
- Die Exposition gegenüber Ergebnisbeziehungen ist schwer zu erkennen.
- Es fehlen Informationen über Störfaktoren.
- Es kann systematische Unterschiede zwischen den Bereichen geben, in denen Expositionen gemessen werden.
Experimentelle Studien
Neben Beobachtungsstudien gibt es auch experimentelle Studien, einschließlich Behandlungsstudien.
Randomisierte kontrollierte Studien

Eine randomisierte kontrollierte Studie (RCT) teilt zufällig Einzelpersonen entweder zu, um eine bestimmte Intervention zu empfangen oder nicht zu erhalten.
Eine von zwei verschiedenen Behandlungen wird verwendet, oder eine Behandlung und ein Placebo.
Dies ist der effektivste Studientyp, um herauszufinden, welche Behandlung am besten funktioniert. Es reduziert den Einfluss externer Variablen.
Die Hauptvorteile von RCTs sind:
- Es gibt keine bewusste oder unbewusste Voreingenommenheit seitens des Forschers. Dies garantiert im Wesentlichen die externe Validität.
- Verwirrende Variablen wie Alter, Geschlecht, Gewicht, Aktivitätsgrad usw. können aufgehoben werden, solange die Beispielgruppe groß genug ist.
Die Hauptnachteile von RCTs sind:
- Sie sind zeitaufwendig.
- Sie können teuer sein.
- Sie erfordern große Beispielgruppen.
- Seltene Ereignisse können schwierig zu lernen sein.
- Es sind sowohl falsch-positive als auch falsch-negative statistische Fehler möglich.
Adaptive klinische Studie
Eine adaptive Entwurfsmethode basiert auf gesammelten Daten. Es ist sowohl flexibel als auch effizient. Änderungen können an der Studie und den statistischen Verfahren laufender klinischer Studien vorgenommen werden.
Quasi-Experiment
Quasi-experimentelle oder "nicht randomisierte" Studien umfassen eine breite Palette von Interventionsstudien, die nicht randomisiert sind. Diese Art von Studie wird häufig verwendet, wenn eine RCT nicht logistisch machbar oder ethisch vertretbar ist.
Hierarchie der Beweise
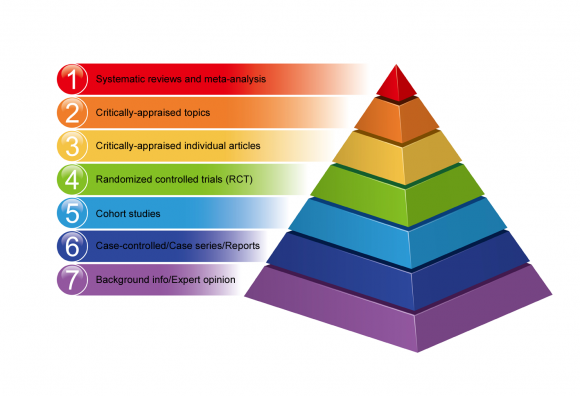
Hierarchien der Evidenz ermöglichen es, verschiedene Forschungsmethoden nach der Validität ihrer Befunde einzustufen.
Nicht alle Forschungsdesigns sind in Bezug auf das Risiko von Fehlern und Verzerrungen in ihren Ergebnissen gleich. Einige Forschungsmethoden liefern bessere Beweise als andere.
Im Folgenden finden Sie ein Beispiel für die Hierarchie der evidenzbasierten Medizin in Form einer Pyramide, die von einer niedrigeren Qualität der Evidenz an der Unterseite bis zu qualitativ hochwertigen Beweisen an der Spitze reicht.
Phasen eines klinischen Tests
Medizinische Forschungsstudien gliedern sich in verschiedene Phasen, sogenannte Phasen. Für Drogentests werden diese von der FDA definiert.
Frühe Phase Studien untersuchen die Sicherheit eines Medikaments und die Nebenwirkungen, die es verursachen kann. Spätere Studien testen, ob eine neue Behandlung besser ist als eine bestehende Behandlung.
Phase-0-Studien: Pharmakodynamik und Pharmakokinetik
Phase 0 ist eine explorative Phase, die hilft, klinische Informationen für ein neues Medikament in einer früheren Phase bereitzustellen.
Diese Phase:
- wird früh in Phase 1 durchgeführt
- beinhaltet sehr begrenzte menschliche Exposition
- hat keine therapeutische oder diagnostische Absicht und beschränkt sich auf Screening- und Mikrodosiestudien
Phase 1 Versuche: Screening für Sicherheit
Nach Phase 0 gibt es beim Menschen vier weitere Versuchsphasen. Diese überschneiden sich oft. Die Phasen 1 bis 3 finden statt, bevor eine Lizenz erteilt wird.
Zu den Leitlinien der Phase 1 gehören:
- zwischen 20 und 80 gesunden Freiwilligen
- Verifizierung der häufigsten Nebenwirkungen des Medikaments
- herauszufinden, wie das Medikament metabolisiert und ausgeschieden wird
Phase-2-Studien: Wirksamkeit feststellen
Wenn Phase-1-Studien keine inakzeptablen Toxizitätswerte ergeben, können Phase-II-Studien beginnen.
Das beinhaltet:
- zwischen 36 und 300 Teilnehmern
- Sammeln vorläufiger Daten darüber, ob das Medikament bei Menschen mit einer bestimmten Krankheit oder Zustand funktioniert
- kontrollierte Studien, um die Personen, die das Medikament erhalten, mit Personen in einer ähnlichen Situation zu vergleichen, die ein anderes Medikament oder ein Placebo erhalten
- kontinuierliche Sicherheitsbewertung
- Studien von kurzfristigen Nebenwirkungen
Phase-3-Studien: Endgültige Bestätigung der Sicherheit und Wirksamkeit
Wenn Phase 2 die Wirksamkeit eines Medikaments bestätigt hat, werden die FDA und die Sponsoren diskutieren, wie in Phase 3 große Studien durchgeführt werden.
Dies beinhaltet:
- zwischen 300 und 3.000 Teilnehmern
- Sammeln weiterer Informationen über Sicherheit und Wirksamkeit
- Studien verschiedener Populationen
- Untersuchung verschiedener Dosierungen, um den besten Verschreibungsbetrag zu bestimmen
- Verwenden des Medikaments in Kombination mit anderen Medikamenten, um die Wirksamkeit zu bestimmen
Nach dieser Phase werden die vollständigen Informationen über das neue Medikament den Gesundheitsbehörden vorgelegt.
Besprechung überprüfen
Wenn die FDA das Produkt für das Marketing genehmigt, werden Post-Marketing-Anforderungen und Verpflichtungsstudien durchgeführt.
Die FDA verwendet diese Studien, um weitere Informationen zur Sicherheit, Wirksamkeit oder optimalen Verwendung des Produkts zu sammeln.
Neue Arzneimittelanwendung

Ein Arzneimittelsponsor wird einen New Drug Application (NDA) ausfüllen, um die FDA zu ersuchen, die Zulassung eines neuen Medikaments zur Vermarktung in den USA zu prüfen.
Eine NDA enthält:
- alle tierischen und menschlichen Daten
- Datenanalyse
- Informationen zum Drogenverhalten im Körper
- Herstellungsdetails
Die FDA hat 60 Tage Zeit, um zu entscheiden, ob sie zur Überprüfung eingereicht werden soll.
Wenn sie sich entscheiden, die NDA einzureichen, wird das FDA-Review-Team beauftragt, die Forschung des Sponsors über die Sicherheit und Wirksamkeit des Medikaments zu bewerten.
Die folgenden Schritte müssen dann stattfinden.
Arzneimittelkennzeichnung: Die FDA überprüft die professionelle Kennzeichnung des Arzneimittels und bestätigt, dass entsprechende Informationen an Verbraucher und Gesundheitsfachkräfte weitergegeben werden.
Anlageninspektion: Die FDA kontrolliert die Einrichtungen, in denen das Medikament hergestellt wird.
Arzneimittelzulassung: FDA-Prüfer genehmigen den Antrag oder geben einen Antwortbrief aus.
Phase-4-Studien: Studien während des Verkaufs
Phase-4-Studien finden statt, nachdem das Medikament für die Vermarktung zugelassen wurde. Sie sind so konzipiert, dass sie beinhalten:
- über 1.000 Patienten
- umfassende Erfahrung in der Bewertung der Sicherheit und Wirksamkeit des neuen Arzneimittels in einer größeren Gruppe und Subpopulationen von Patienten
- Vergleich und Kombination mit anderen verfügbaren Behandlungen
- Bewertung der langfristigen Nebenwirkungen des Arzneimittels
- Erkennung von weniger häufigen unerwünschten Ereignissen
- Kosteneffektivität der medikamentösen Therapie im Vergleich zu anderen traditionellen und neuen Therapien
Sicherheitsbericht
Nachdem die FDA ein Medikament genehmigt hat, beginnt das Post-Marketing-Stadium. Der Sponsor, in der Regel der Hersteller, übermittelt der FDA regelmäßig Sicherheitsupdates.
Wer sponsert klinische Studien?
Klinische Studien und Forschung können Hunderte von Millionen Dollar kosten. Gruppen, die Studien finanzieren, können Folgendes umfassen:
- Pharma-, Biotechnologie- und Medizintechnikunternehmen
- akademische medizinische Zentren
- freiwillige Gruppen und Stiftungen
- Nationales Gesundheitsinstitut
- Regierungs Einrichtungen
- Ärzte und Gesundheitsdienstleister
- Einzelpersonen
Wer kann teilnehmen?
Das Protokoll definiert, wer berechtigt ist, an einer Studie teilzunehmen.
Mögliche Einschlusskriterien können sein:
- eine bestimmte Krankheit oder einen bestimmten Zustand haben
- gesund sein, ohne Gesundheitszustand
Ausschlusskriterien sind die Faktoren, die manche Menschen davon abhalten, an einer Studie teilzunehmen.
Beispiele sind Alter, Geschlecht, ein bestimmter Typ oder ein bestimmtes Stadium einer Krankheit, frühere Behandlungsanamnese und andere medizinische Bedingungen.
Mögliche Vorteile und Risiken
Die Teilnahme an klinischen Studien kann sowohl Vorteile als auch Risiken für die Teilnehmer mit sich bringen.
Mögliche Vorteile klinischer Studien umfassen Folgendes:
- Die Teilnehmer haben Zugang zu neuen Behandlungen.
- Wenn eine Behandlung erfolgreich ist, werden die Teilnehmer zu den Ersten gehören, die davon profitieren.
- Teilnehmer, die nicht in der Gruppe sind, die eine neue Behandlung erhalten, können die Standardbehandlung für den bestimmten Zustand erhalten, die genauso gut oder besser als der neue Ansatz sein kann.
- Die Gesundheit wird von einem Team von Gesundheitsdienstleistern genau überwacht und unterstützt.
- Informationen aus klinischen Studien tragen zu wissenschaftlichen Erkenntnissen bei, können anderen helfen und verbessern letztendlich die Gesundheitsversorgung.
Mögliche Risiken sind:
- Die Standardversorgung für einen bestimmten Zustand kann manchmal besser sein als die neue Strategie oder Behandlungen, die untersucht werden.
- Der neue Ansatz oder die Behandlung kann für einige Teilnehmer gut funktionieren, aber nicht unbedingt für andere.
- Es kann unerwartete oder unvorhergesehene Nebenwirkungen geben, insbesondere in Phase-1- und Phase-2-Studien und bei Ansätzen wie Gentherapie oder neuen biologischen Behandlungen.
- Krankenkassen und Gesundheitsdienstleister decken nicht immer die Patientenversorgung und Kosten für diejenigen, die an klinischen Studien teilnehmen.
Was bedeutet Zustimmung?

Das Einverständniserklärungsdokument erläutert die Risiken und potenziellen Vorteile der Teilnahme an einer klinischen Prüfung.
Zu den Elementen, die im Dokument erscheinen müssen, gehören unter anderem:
- Zweck der Forschung
- vorhersehbare Risiken von Beschwerden
- mögliche Vorteile
Von den Teilnehmern wird erwartet, dass sie das Einwilligungsdokument gründlich lesen und entscheiden, ob sie sich anmelden und unterschreiben möchten, bevor sie in die Studie aufgenommen werden können.
Sind klinische Studien sicher?
Die FDA stellt sicher, dass jeder, der eine Studie in Erwägung zieht, Zugang zu allen zuverlässigen Informationen hat, die er für eine fundierte Entscheidung benötigt, einschließlich Informationen über die Risiken.
Während die Risiken für die Teilnehmer kontrolliert und überwacht werden, können aufgrund der Art der medizinischen Forschungsstudien gewisse Risiken unvermeidlich sein.
Wie sind die Teilnehmer geschützt?

Die Sicherheit der Teilnehmer ist ein vorrangiges Thema. In jedem Versuch tragen wissenschaftliche Aufsicht und Patientenrechte zu ihrem Schutz bei.
Good Clinical Practice (GCP) soll sicherstellen, dass ethische und angemessene Verfahren in Studien eingehalten werden.
Die Einhaltung der GCP gibt der Öffentlichkeit das Vertrauen, dass die Sicherheit und die Rechte der Teilnehmer geschützt sind.
Es zielt darauf ab:
- um die Rechte, die Sicherheit und das Wohlergehen der Teilnehmer zu schützen
- sicherzustellen, dass die erhobenen Daten zuverlässig sind, Integrität aufweisen und von angemessener Qualität sind
- Richtlinien und Standards für die Durchführung klinischer Forschung bereitzustellen
Die Grundlagen von GCP wurden erstmals im Jahr 1947 gelegt. Die wichtigsten Punkte waren, dass Forscher während jeder Studie garantieren müssen:
- freiwillige Teilnahme
- Einverständniserklärung
- Minimierung des Risikos
Mit der Zeit reichten die Ergänzungen von der Schaffung zusätzlichen Schutzes für gefährdete Bevölkerungsgruppen bis hin zur Bereitstellung von Leitlinien für Forschungseinrichtungen.
Patientenrechte
Wege zum Schutz der Patientenrechte schließen die folgenden ein:
Einwilligung nach Aufklärung ist der Prozess, bei dem die Teilnehmer der klinischen Prüfung mit allen Fakten über die Studie versorgt werden. Dies geschieht vor der Teilnahme der Teilnehmer und während des Prozesses. Die Einwilligungserklärung enthält Einzelheiten über die möglichen Behandlungen und Tests sowie die möglichen Vorteile und Risiken.
Andere Rechte: Das Einwilligungsdokument ist kein Vertrag; Teilnehmer können jederzeit aus der Studie austreten, unabhängig davon, ob die Studie abgeschlossen ist oder nicht.
Rechte und Schutz für Kinder: Ein Elternteil oder Erziehungsberechtigter muss seine Zustimmung erteilen, wenn das Kind 18 Jahre oder jünger ist. Wenn eine Studie ein Risiko beinhaltet, das größer als minimal ist, müssen beide Elternteile ihre Zustimmung geben. Kinder über 7 Jahren müssen zustimmen, an klinischen Studien teilzunehmen.
Wie finde ich eine klinische Studie?
Informationen über aktuelle klinische Studien finden Sie hier.